Covid-19: le vaccin Pfizer/BioNTech approuvé par l'Agence européenne des médicaments
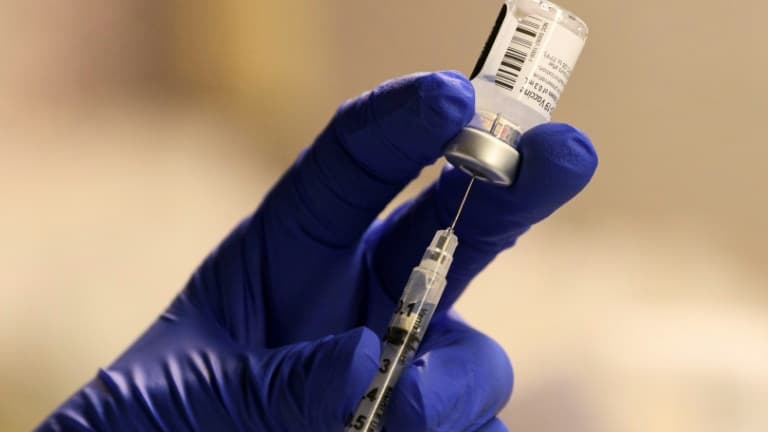
Une infirmière prépare une dose du vaccin Pfizer-BioNTech contre le Covid-19 dans un centre de vaccination à Torrance, le 19 décembre 2020 en Californie - Patrick T. Fallon © 2019 AFP
L'Europe ouvre à son tour ses portes au vaccin contre le Covid-19. L'Agence européenne des médicaments (EMA), basée à Amsterdam, a annoncé ce lundi qu'elle autorisait le vaccin Pfizer-BioNTech. La liste des pays ayant donné leur accord à ce sérum s'allonge donc encore: l'Europe rejoint le Royaume-Uni, les Etats-Unis, le Canada, Bahreïn, l'Arabie saoudite, le Mexique, Singapour, Israël et la Suisse.
Réservé aux plus de 16 ans
"Je suis ravie d'annoncer que le comité scientifique de l'AEM s'est réuni aujourd'hui et s'est montré favorable à une autorisation de mise sur le marché conditionnelle dans l'UE pour le vaccin développé par Pfizer et BioNTech", a déclaré la directrice générale de l'AEM, Emer Cooke, au cours d'une conférence de presse en ligne.
Mais l'EMA a cependant fixé des conditions à l'administration du vaccin, notamment celle d'être âgé de plus de 16 ans.
"Un moment décisif"
La Commission européenne doit désormais approuver cette décision afin de lancer la campagne de vaccination dans l'ensemble de l'Union européenne qui compte près de 450 millions d'habitants.
"C'est un moment décisif dans les efforts que nous fournissons pour diffuser un vaccin sûr et efficace aux Européens. Nous allons agir vite. J'attends une décision de la Commission européenne dans la soirée", a tweeté dans la foulée Ursula Von der Leyen, la présidente de la commission.
Décision avancée
Pfizer-BioNTech avait rempli une demande d'autorisation le 1er décembre et l'AEM avait réagi, indiquant qu'elle prendrait sa décision le 29 décembre lors d'une réunion d'experts.
Mais plusieurs Etats s'étaient plaints d'un délai de prise de décision trop lent après un sommet européen au cours duquel les dirigeants polonais et hongrois avaient appelé l'EMA à accélérer. Berlin avait appuyé de tout son poids les appels lancés plus tôt par la Hongrie et la Pologne pour une décision plus rapide.
L'Agence européenne des médicaments avait en réaction avancé la date d'annonce de sa décision de huit jours, la déplaçant ainsi au 21 décembre.









